目前,由于抗生素的大量使用以及新型抗生素研发的迟缓,细菌耐药性目前已经对全球公众健康以及经济发展产生了巨大威胁。由于细胞膜合成涉及复杂的生化过程,因此膜靶向的抗菌高分子化合物一般具有很低的耐药性,也因此受到了广泛关注。
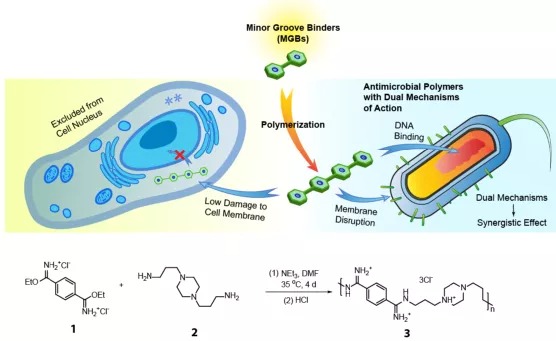
该领域先前的研究主要集中在抗菌聚合物的结构筛选和构效关系研究上,以期能够获得具有更好治疗指数(TI)的聚合物。但是,由于真核细胞和细菌细胞膜结构的相似性,抗菌高分子很容易对真核细胞的细胞膜也造成一定程度的破坏,产生不可忽略的真和细胞毒性,这对它们的应用产生了很大的限制。近日,湖南大学冯欣欣课题组、白玉罡课题组在 Science 子刊 Science Advances 杂志发表了题为:A polymeric approach toward resistance-resistant antimicrobial agent with dual-selective mechanisms of action 的研究论文。冯欣欣、白玉罡教授课题组提出了“双重机理”策略来提升抗菌高分子的选择性,即在抗菌聚合物的分子结构中引入靶向细菌DNA的第二重抗菌机制。
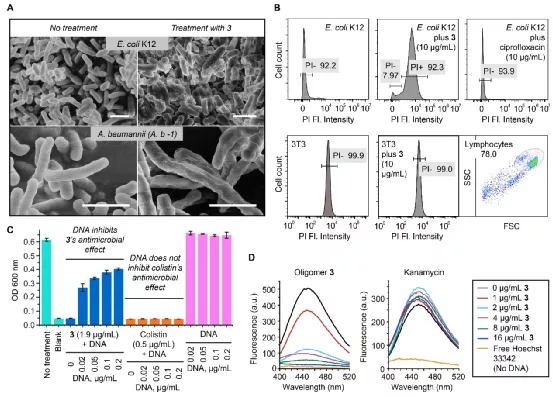
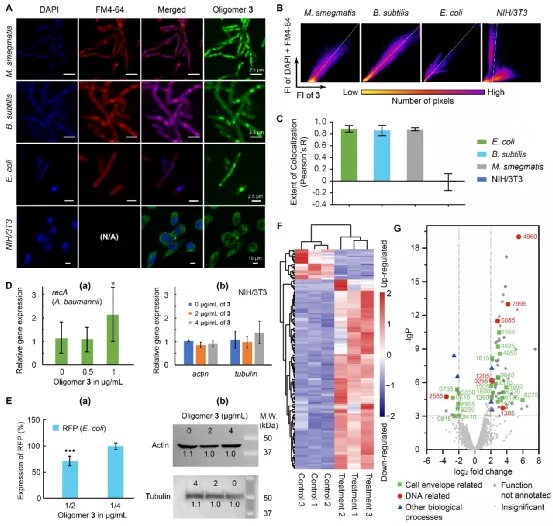
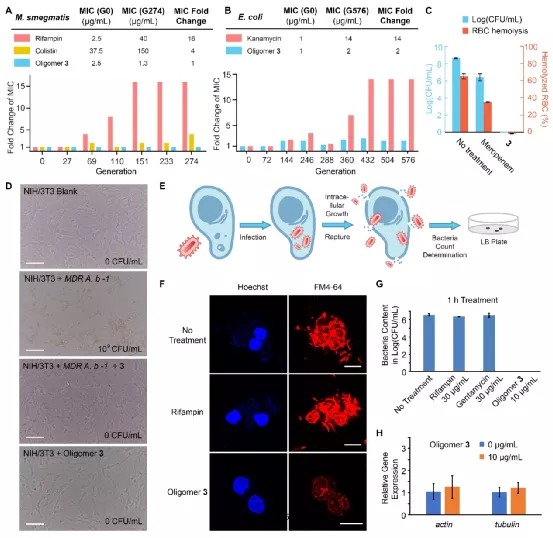
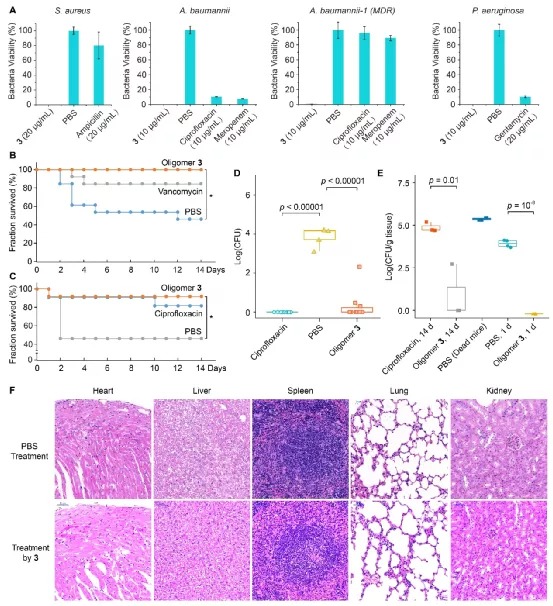
众所周知,细菌DNA位于无膜保护的拟核中,而真核细胞的DNA位于细胞核中,受到核膜的保护,因此这一物种上的显著差异性就可以用来产生选择性。核膜本质上是一个半透膜,除了通过细胞自身的转运机制之外,其他分子在分子量大到一定程度之后就会被核膜屏蔽在外。基于此,该课题组率先报导了一种寡聚脒类聚合物,该寡聚物能够选择性地破坏细菌细胞膜的完整性,同时选择性地只与细菌DNA结合,从而通过双重选择性机理得到更高的治疗指数。为引入DNA结合机理,该研究团队选择了双脒结构作为结合DNA沟槽结构,从而获得了一个既提供阳离子,也能够绑定DNA沟槽的聚合物。同时,这种通过缩聚方式合成的寡聚脒的分子量也足够大,令其无法进入真核细胞的细胞核。这样的结构便可以产生出具有更好选择性的DNA结合型抗菌机制,这种新型机理能同膜靶向机制结合起来,在保证抗菌效果的前提下降低其真核细胞毒性。该团队利用对苯二甲亚胺酸乙酯和各种二胺缩聚合成了一系列寡聚脒类聚合物,经过初步的抗菌以及溶血性能筛选,从一系列的寡聚物中选择了效果最好的化合物——寡聚物3进行进一步的研究。经过一系列耐药性细菌的抑菌以及杀菌实验和细胞毒性实验,研究团队进一步确定了寡聚物3在体外具有优异的抗菌活性以及生物安全性。随后,研究团队研究了寡聚物3的抗菌机理,验证3的结构设计是否真正实现了原核细胞选择性。通过SEM、流式细胞术、进胞机理等一系列实验,研究团队确定了寡聚物3可以选择性地破坏细菌的细胞膜。从3的结构可以看出,它的电荷密度较高,亲油部分很少,显然具有较弱的膜结合能力;但考虑到其高正电性,它对负电性更强的细菌膜就仍然有较好的结合与破坏能力。由此,寡聚物3的第一重选择性抗菌机理就得到了验证。(A) 寡聚物3处理大肠杆菌(K12)(上)和MDR Acinetobacter baumannii -1(下)有明显的膜损伤 (B)大肠杆菌和3T3细胞的碘化丙啶(PI)膜透性试验表明寡聚物3选择性破坏细菌细胞膜。(C)寡聚物3的细胞内化机制。(D) 外源添加DNA抑制寡聚物3的活性。(E) 荧光竞争实验表明寡聚物 3能够结合DNA小沟槽研究团队随后利用DNA拯救实验、荧光竞争实验以及计算化学方法等进一步证明了寡聚物3能够特异性结合DNA小沟,并进一步对寡聚物3在细菌和真核细胞的DNA选择性上又进行了更深入的研究。研究团队合成了荧光标记的寡聚物3,观察了它在细菌和真核细胞中的分布,实验结果证明了寡聚物3能够很好地与细菌DNA结合,却无法进入哺乳动物细胞核。在此基础上,团队还使用RT-PCR实验、转录组分析以及Western blot实验在转录和翻译层面证明了寡聚物3的DNA结合机理的选择性。(A) DAPI、FM4-64和3-FITC染色的细菌和哺乳动物细胞共聚焦显微图像。(B)染色细菌和哺乳动物细胞的二维荧光强度直方图。(C)膜和DNA染色与3-FITC染色的Pearson’s相关系数R。(D) 寡聚物3选择性激活细菌内的管家基因。(E) 寡聚物3选择性抑制细菌蛋白表达。(F) 鲍曼不动杆菌经寡聚物3处理后的差异表达分析热图。(G)鲍曼不动杆菌经寡聚物3处理后的转录组结果火山图A/B) 与小分子抗生素不同,寡聚物3很难使细菌产生抗药性。(C)寡聚物3可以在红细胞存在的条件下完全杀死细菌,并不产生溶血,其效果优于传统抗生素美洛培南。(D)寡聚物3可以在NIH/3T3细胞存在的条件下完全杀死耐药性细菌,拯救被感染的细胞。(E)细菌的胞内感染模型示意图。(F)寡聚物3可以杀死巨噬细胞内的细菌,并不对巨噬细胞产生明显影响。(G)寡聚物3的胞内抗菌效果定量图。(H)寡聚物3在胞内抗菌条件下不对巨噬细胞的基因表达产生影响研究团队随后建立了一系列细胞感染模型,在这些真核细胞与细菌共存的模型实验中,寡聚物3能够有效杀灭复杂模型中的细菌同时保护细胞不受伤害。更重要的是,由于寡聚物3可以进入细胞当中(但不进入细胞核),它可以杀死细胞内隐藏的细菌,这比起许多传统小分子抗生素来说是一个很大的优势。同时,由于寡聚物3仍然具有膜靶向机理,它和传统的膜靶向抗菌高分子一样,具有不易产生耐药性这一特性。在后续的动物实验中,研究团队用线虫和小鼠建立了几种不同的模型,尝试了线虫感染模型、小鼠皮肤脓肿模型以及小鼠外切伤口模型。在这些实验中,明寡聚物3均显示了很好的杀菌效果,能够有效杀灭创面和体内的细菌,显著提高受到严重细菌感染的动物的存活率。小鼠解剖切片结果显示,在治疗过程中寡聚物3未对动物机体产生明显的毒性。(A)寡聚物3在不同细菌的线虫感染模型中疗效。(B) 小鼠皮肤脓肿感染模型中不同药物处理的存活率。(C)小鼠外切伤口模型中不同药物处理的存活率。(D) 小鼠外切伤口模型中,寡聚物3能显著减少感染区域的细菌数量。(E) 小鼠外切伤口模型中,寡聚物3可以有效地抑制被感染老鼠各个器官中的细菌繁殖。(F)组织免疫组织学切片图像。总体来说,该研究为新型抗菌高分子的开发提供了全新的策略与思路。研究团队通过合理结构设计,实现了具有双重作用机制的抗菌聚合物的合成,并且该聚合物的两种抗菌机理均具有原核细胞选择性,这种内在的协同作用使得聚合物具备高性能、低毒性和低耐药性。论文的第一作者为湖南大学化学化工学院冯欣欣、白玉罡课题组联培博士生白思蕾,共同第一作者为白玉罡课题组博士生王建雪、冯欣欣课题组硕士生杨凯玲,通讯作者为湖南大学化学化工学院冯欣欣副教授和白玉罡教授。https://advances.sciencemag.org/content/7/5/eabc9917